Перейти к:
Изучение нейропротекторного действие дипептидных миметиков NT-3 соединений ГТС-301 и ГТС-302 на экспериментальной модели ишемического инсульта
https://doi.org/10.37489/2587-7836-2026-1-12-19
EDN: LPQHXJ
Аннотация
Инсульт является одной из основных причин смертности и инвалидизации в мире, в связи с чем актуальна разработка новых средств его фармакотерапии. Белки семейства нейротрофинов (NGF, BDNF, NT-3, NT-4) являются эндогенными нейропротекторами, а также способствуют нейрорегенерации. Проблемы клинического применения нейротрофинов (низкая биодоступность, риск развития побочных эффектов) могут быть преодолены с помощью создания их фармакологически пригодных низкомолекулярных миметиков. В ФГБНУ «ФИЦ оригинальных и перспективных биомедицинских и фармацевтических технологий» были сконструированы и синтезированы на основе β-изгиба 4-й петли NT-3 его димерные дипептидные миметики соединения ГТС-301 (гексаметилендиамид бис-(N-моносукцинил-L-аспарагинил-L-аспарагина)) и ГТС-302 (гексаметилендиамид бис-(N-γ-оксибутирилL-глутамил-L-аспарагина)).
Целью настоящего исследования было выявление возможной нейропротекторной активности у ГТС-301 и ГТС-302 на модели ишемического инсульта на крысах, индуцированного окклюзией средней мозговой артерии (ОСМА). Дипептиды вводили внутрибрюшинно в дозе 1 мг/кг в течение 7 дней, первое введение было через 4 ч после моделирования ОСМА. На 3-и и 6-е сутки оценивали неврологический статус животных в тесте стимулирования конечностей, на 7-е сутки регистрировали объём инфаркта мозга с помощью морфометрии срезов, окрашенных хлоридом 2,3,5-трифенилтетразолия. Результаты. Было установлено, что ГТС-302 снижает объём инфаркта мозга на 39 % по сравнению с нелечеными животными и статистически значимо улучшает неврологический статус на 3-и сутки после ОСМА. Соединение ГТС-301 было не активно. Различия в активности изученных соединений на модели ОСМА могут быть связаны с тем, что, как было ранее установлено in vitro, ГТС-302 активирует, подобно полноразмерному NT-3, все основные пути трансдукции сигнала нейротрофиновых Trk рецепторов — PI3K/Akt, MAPK/ERK и PLC-γ1, а ГТС-301 — только MAPK/ERK и PLC-γ1. Полученные в настоящем исследовании данные, а также результаты ранее проведённых нами исследований нейропротекторной активности дипептидных миметиков NGF и BDNF в тех же условиях свидетельствуют о важности активации PI3K/Akt для проявления нейропротекторной активности дипептидных миметиков нейротрофинов на модели ОСМА.
Ключевые слова
Для цитирования:
Никифоров Д.М., Поварнина П.Ю., Гудашева Т.А. Изучение нейропротекторного действие дипептидных миметиков NT-3 соединений ГТС-301 и ГТС-302 на экспериментальной модели ишемического инсульта. Фармакокинетика и Фармакодинамика. 2026;(1):12-19. https://doi.org/10.37489/2587-7836-2026-1-12-19. EDN: LPQHXJ
For citation:
Nikiforov D.M., Povarnina P.Yu., Gudasheva T.A. Study of the neuroprotective effect of NT-3 dipeptide mimetics GTS-301 and GTS-302 on an experimental model of ischemic stroke. Pharmacokinetics and Pharmacodynamics. 2026;(1):12-19. (In Russ.) https://doi.org/10.37489/2587-7836-2026-1-12-19. EDN: LPQHXJ
Введение
Инсульт является второй по распространённости среди неинфекционных заболеваний причиной смертности и одной из основных причин инвалидизации в мире. В 2021 году было зарегистрировано около 12 миллионов инсультов, больше половины из которых привели к смерти [1]. Такая неутешительная статистика демонстрирует актуальность разработки новых средств фармакотерапии инсульта. В этой связи большое внимание привлекают эндогенные белки семейства нейротрофинов (NGF, BDNF, NT-3, NT-4), обладающие нейропротекторными и нейрорегенеративными свойствами [2, 3].
Физиологические эффекты нейротрофинов в основном опосредованы специфическими тирозинкиназными Trk рецепторами — TrkA, TrkB и TrkC [4]. Разные популяции нейронов экспрессируют все или только отдельные типы Trk рецепторов, при этом большинство нейронов экспрессирует хотя бы один тип этих рецепторов [5, 6]. В отличие от других нейротрофинов, NT-3 взаимодействует не только со своими специфическими TrkC рецепторами, но также с TrkA и TrkB [7], что свидетельствует о возможности нейропротекции в отношении большинства популяций нейронов.
Нейропротекторные эффекты NT-3 были выявлены на in vivo модели ишемического инсульта, индуцированного окклюзией средней мозговой артерии (ОСМА). В работе [8] было показано, что внутримозговое введение крысам вирусного вектора, несущего ген NT-3, за 3 дня до моделирования ОСМА приводило к снижению объёма инфаркта мозга на 40 % и к улучшению неврологического статуса с 1-го по 28-й день после операции. Нанесение NT-3 (10 мкг в физиологическом растворе) на поверхность повреждённого полушария мозга крыс во время моделирования ОСМА способствовало снижению объёма ишемического повреждения на 60 % по сравнению с нелечеными животными, а также значительно снижало некроз и апоптоз в ишемизированной области [9]. У NT-3 были выявлены также нейрорегенеративные эффекты на модели ишемического повреждения сенсомоторной коры крыс, представляющей переднюю лапу [10]. Было установлено, что введение NT-3 в составе вирусного вектора в мышцы повреждённой лапы через 24 ч после моделирования ишемии способствовало прорастанию аксонов кортикоспинальных нейронов из коры неповреждённого полушария в спинной мозг, что сопровождалось восстановлением чувствительности и двигательных функций повреждённой передней лапы [10]. В исследованиях in vitro было показано, что ингибирование экспрессии NT-3 в культуре крысиных кортикальных нейронов в условиях кислородно-глюкозного голодания усиливает их апоптоз [11]. Эти данные также свидетельствуют о нейропротекторных свойствах NT-3 при церебральной ишемии.
Поскольку клиническое применение нейротрофинов ограничено их низкой биодоступностью и риском развития серьёзных побочных эффектов [12, 13], рядом исследовательских групп разрабатываются их низкомолекулярные фармакологически пригодные миметики. В то время как некоторые низкомолекулярные миметики NGF и BDNF хорошо охарактеризованы и находятся на стадиях доклинических и клинических исследований как средства лечения неврологических заболеваний [14], в доступной литературе на настоящий момент нет данных об in vivo эффектах миметиков NT-3.
В лаборатории пептидных биорегуляторов ФГБНУ «ФИЦ оригинальных и перспективных биомедицинских и фармацевтических технологий» были сконструированы и синтезированы два димерных дипептидных миметика NT-3 — ГТС-301 и ГТС-302 [15, 16]. В экспериментах in vitro на клетках PC12, экспрессирующих TrkC рецепторы, было показано, что ГТС-302, подобно полноразмерному NT-3, активирует все основные сигнальные каскады Trk-рецепторов: PI3K/Akt, MAPK/ERK и PLC-γ1. ГТС-301, в свою очередь, активирует только MAPK/ERK и PLC-γ1, не влияя на PI3K/Akt [17].
Целью настоящего исследования было выявление нейропротекторной активности соединений ГТС-301 и ГТС-302 на модели ишемического инсульта у крыс, вызванного ОСМА.
Материалы и методы
Химические вещества и реагенты.
Дипептиды ГТС-301 (гексаметилендиамид бис-(N-моносукцинил-L-аспарагинил-L-аспарагина)) и ГТС-302 (гексаметилендиамид бис-(N-γ-оксибутирил-L-глутамил-L-аспарагина)) были получены в лаборатории пептидных биорегуляторов отдела химии лекарственных средств ФГБНУ «ФИЦ оригинальных и перспективных биомедицинских и фармацевтических технологий» как описано в работах [15, 16]. Хлоралгидрат и формалин — производства PanReac Applichem (США), хлорид 2,3,5-трифенилтетразолия (ТТХ) — производства HiMedia Laboratories (Индия), Tween-80 — производства ICN Biomedicals (США).
Животные.
Исследование проведено на 33 крысах-самцах линии Wistar массой 230–260 г, полученных из Филиала «Андреевка» ФГБУН «Научный центр биомедицинских технологий» ФМБА России. Животных содержали в условиях вивария при свободном доступе к пище и воде и при естественной смене светового режима. Эксперименты с животными проводили в соответствии с Решением Совета Евразийской экономической комиссии от 3 ноября 2016 г. № 81 «Об утверждении Правил надлежащей лабораторной практики Евразийского экономического союза в сфере обращения лекарственных средств», межгосударственным стандартам серии «Руководство по содержанию и уходу за лабораторными животными» ГОСТ 33215-2014 и ГОСТ 33216-2014 (Приложение А к Европейской конвенции о защите позвоночных животных, используемых в экспериментах и в других научных целях (ETS N 123)). Проведение исследования одобрено Комиссией по биомедицинской этике ФГБНУ «ФИЦ оригинальных и перспективных биомедицинских и фармацевтических технологий» (протокол № 2 от 30 января 2023 г.).
Моделирование ишемического инсульта.
Ишемический инсульт моделировали с помощью внутрисосудистой транзиторной ОСМА [18]. Все хирургические манипуляции осуществлялись с помощью титановых микрохирургических инструментов. Животных вводили в наркоз с помощью 5 % раствора хлоралгидрата в физиологическом растворе (350 мг/кг, в/б). Производили срединный разрез в вентральной области шеи и выделяли с правой стороны сонный треугольник, образованный сверху двубрюшной мышцей, латерально — грудино-ключично-сосцевидной мышцей и медиально — грудино-подъязычной мышцей. Затем грудино-подъязычную и грудино-подъязычно-сосцевидную мышцы рассекали, для того чтобы открыть доступ к общей сонной артерии. Осторожно отделяли от сонной артерии блуждающий нерв и временно накладывали микрохирургическую сосудистую клипсу на 1,5 см ниже её бифуркации. Далее аккуратно выделяли из тканевых спаек внешнюю и внутреннюю сонные артерии. Внешнюю сонную артерию необратимо перекрывали при помощи хлопчатобумажной нити на расстоянии 0,5 см от бифуркации. Изолировали крылонёбную артерию от сопутствующих тканей и коагулировали её электрокаутером для предотвращения чрезмерного кровотечения. На внутреннюю сонную артерию временно накладывали викриловую нить и неплотно затягивали, после чего перерезали внешнюю сонную артерию проксимальнее наложения хлопчатобумажной нити. Через образовавшуюся после разреза культю проводили монофиламент, представлявший собой нейлоновую нить диаметром 0,25 мм, которая на 2/3 длины была покрыта силиконом. Ослабляли узел викриловой нити на внутренней сонной артерии и продвигали монофиламент по сосуду на расстояние 19–21 мм от бифуркации до перекрытия средней мозговой артерии, после чего фиксировали его микрососудистой клипсой. Время перекрытия средней мозговой артерии составляло 60 мин, по истечении которых монофиламент аккуратно медленно извлекали из сосуда, разрез внешней сонной артерии закрывали путём коагуляции электрокаутером до полной герметичности. Внутреннюю сонную артерию освобождали от викриловой нити, а ствол общей сонной артерии — от микрососудистого зажима, что приводило к полной реперфузии.
Ложнооперированные животные подвергались тем же хирургическим манипуляциям, за исключением перерезания внешней сонной артерии и введения монофиламента. Срединный разрез шеи зашивали хлопчатобумажной нитью и обрабатывали стрептоцидом. Температуру тела животных во время операции и до выхода из наркоза поддерживали на уровне 37 °С при помощи согревающего коврика.
Крыс случайным образом разделили на 4 группы: ложная операция (ЛО, *n* = 8), окклюзия средней мозговой артерии (ОСМА, *n* = 8), ОСМА+ГТС-301 (*n* = 8) и ОСМА+ГТС-302 (*n* = 9). Дипептид ГТС-302 растворяли в воде для инъекций; ГТС-301 ввиду его плохой растворимости в воде суспензировали в 1 % растворе Tween-80 в воде для инъекций. Доза ГТС-302 (1 мг/кг, внутрибрюшинно (в/б)) была выбрана на основании ранее проведённых исследований его фармакологической активности [12], ГТС-301 вводили в той же дозе (1 мг/кг, в/б). Дипептиды вводили в/б 1 раз в день в течение 7 суток, первое введение было через 4 ч после моделирования инсульта. Крысы из групп ЛО и ОСМА получали в том же режиме воду для инъекций. Объём введения составлял 2 мл на 1 кг массы тела крыс. На 3-и и 6-е сутки после операции регистрировали неврологический статус. На 7-е сутки определяли объём инфаркта мозга. Дизайн исследования приведён на рисунке 1.

Рис. 1. Дизайн исследования
Примечание: ОСМА — окклюзия средней мозговой артерии.
Регистрация неврологического дефицита.
Неврологический дефицит оценивали в модифицированном тесте стимулирования конечностей [19], который изначально был описан De Ryck M, et al. [20]. Данный тест заключается в оценке ответа задних и передних конечностей на тактильную и проприоцептивную стимуляцию и состоит из 7 различных испытаний для левой и правой стороны тела. Испытания оценивались следующим образом:
крыса выполнила испытание полностью и без задержки — 2 балла;
крыса выполнила испытание не полностью или с задержкой не больше 2 с — 1 балл;
крыса не выполнила испытание — 0 баллов.
Для каждого животного подсчитывалась сумма баллов для левой и правой стороны тела. Максимальное количество баллов для каждой стороны тела — 14, что соответствует отсутствию неврологических нарушений.
Определение объёма инфаркта мозга.
Объём ишемического повреждения оценивали с помощью морфометрии срезов мозга, окрашенных хлоридом 2,3,5-трифенилтетразолия (ТТХ) [21]. Животных вводили в глубокий наркоз 5 % раствором хлоралгидрата (350 мг/кг, в/б), после чего декапитировали. Головной мозг извлекали и помещали, чтобы отмыть от крови, на 1 мин в ёмкость с физиологическим раствором. Затем мозг замораживали при –20 °С в течение 12 мин и с помощью специальной формы с пазами для точной резки и микротомных лезвий разрезали на 5 фронтальных срезов толщиной 1,2 мм. Срезы мозга помещали в чашку Петри с 2 % раствором ТТХ в фосфатно-солевом буфере и инкубировали в течение 15 мин при 37 °С, переворачивали и инкубировали в тех же условиях ещё 15 мин, после чего фиксировали в 10 % формалине в течение 30 мин. Затем срезы помещали на предметные стёкла и сканировали с двух сторон с помощью планшетного сканера с разрешением 2400 dpi в режиме цветного изображения. С помощью свободно распространяемой программы Image J (National Institutes of Health, США) измеряли площадь инфаркта (неокрашенная область), а также площади ишемизированного и интактного полушарий.
Для исключения погрешностей измерения, связанных с отёком или атрофией ткани в ишемизированном полушарии, рассчитывали относительный объём инфаркта по следующей формуле:
V=Vin×(Vc/Vi)Vc×100%
где Vin — объём инфаркта мозга; Vi — объём ипсилатерального полушария; Vc — объём контралатерального полушария [22].
Статистический анализ данных проводили с помощью компьютерной программы GraphPad Prism 8.0 (GraphPad Software, США). В связи с небольшим объёмом выборок использовали непараметрическую статистику. Для сравнения групп использовали критерий Краскела–Уоллиса с последующим тестом Данна или U-тест Манна–Уитни с поправкой Бенджамини–Хохберга. Различия считали статистически значимыми при p < 0,05.
Результаты и обсуждение
В первые сутки после операции погибло 3 животных из 8 в группе «ОСМА», 4 из 8 в группе «ОСМА+ГТС-301» и 1 из 9 в группе «ОСМА+ГТС-302»; среди ложнооперированных животных гибели не было. Одна крыса из группы «ОСМА» была исключена из исследования в связи с неудачным моделированием инсульта (отсутствовал неврологический дефицит и инфаркт мозга).
В тесте стимулирования конечностей у ложнооперированных крыс не наблюдалось неврологического дефицита как с левой, так и с правой стороны тела — суммарное число баллов у всех животных было 14 для каждой из сторон тела на 3-и и 6-е сутки после операции. У крыс из групп «ОСМА», «ОСМА+ГТС-301» и «ОСМА+ГТС-302» суммарное число баллов для правой (ипсилатеральной повреждению) стороны тела также составляло 14 на 3-и и 6-е сутки после операции, однако у всех животных наблюдался неврологический дефицит для левой (контрлатеральной повреждению) стороны тела. В группе «ОСМА» суммарное число баллов для левой стороны тела на 3-и и 6-е сутки составляло в среднем (± стандартная ошибка среднего) 8±0,7 (p = 0,0008 по сравнению с группой «ложная операция») и 9±0,8 (p = 0,0008 по сравнению с группой «ложная операция») соответственно (рис. 2). Введение ГТС-302 приводило к статистически значимому улучшению неврологического статуса на 3-и сутки после операции: число баллов в группе «ОСМА+ГТС-302» составляло 10,2±0,4 (p = 0,018 по сравнению с группой «ОСМА») (см. рис. 2). На 6-е сутки эффект ГТС-302 не достигал статистической значимости (число баллов 10,9±0,5). У ГТС-301 не было выявлено статистически значимого эффекта на неврологический статус крыс.
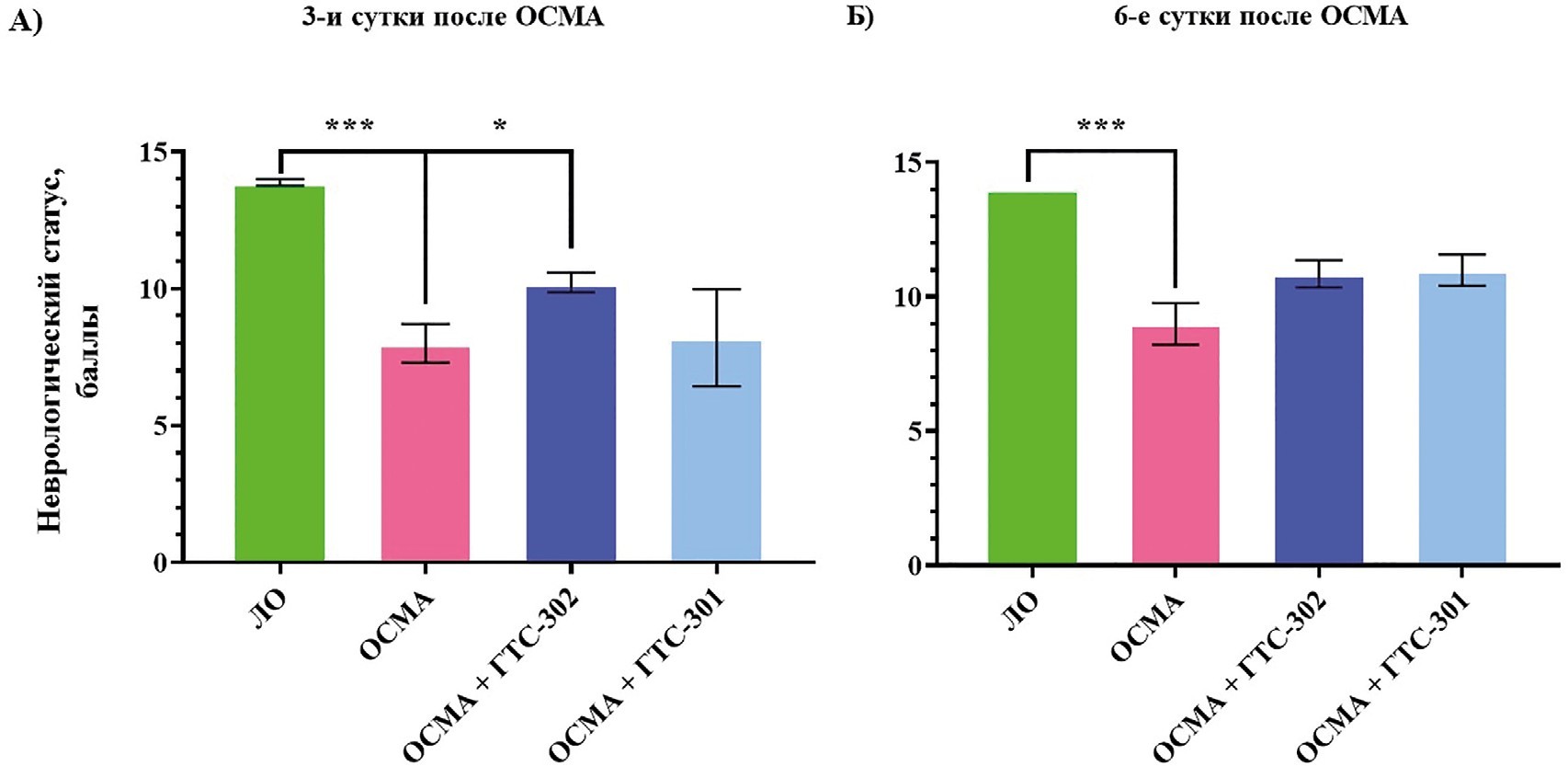
Рис. 2. Неврологический статус крыс в тесте стимулирования конечностей после ОСМА
Примечания: Сумма баллов для левой (контрлатеральной повреждению) стороны тела. А — на 3-й день после ОСМА; Б — на 6-й день после ОСМА. Данные представлены в виде средних значений и стандартных ошибок среднего. *** — p < 0,001 по сравнению с группой ЛО; * — p < 0,05 по сравнению с группой ОСМА (U-тест Манна–Уитни с поправкой Бенджамини–Хохберга).
У крыс из группы «ОСМА» на срезах мозга, окрашенных хлоридом 2,3,5-трифенилтетразолия, регистрировалась выраженная область инфаркта (неокрашенная зона), захватывающая кору и стриатум правого полушария (рис. 3), объём которой составлял в среднем 34,7±2,8 % относительно интактного полушария. Введение ГТС-302 приводило к статистически значимому (p = 0,0177 по сравнению с группой «ОСМА») снижению объёма инфаркта мозга на 39 % (до 21,3±2,9 %). Дипептид ГТС-301 не оказывал статистически значимого эффекта, объём инфаркта мозга в группе «ОСМА+ГТС-301» составлял 28,7±5,4 % от интактного полушария мозга.
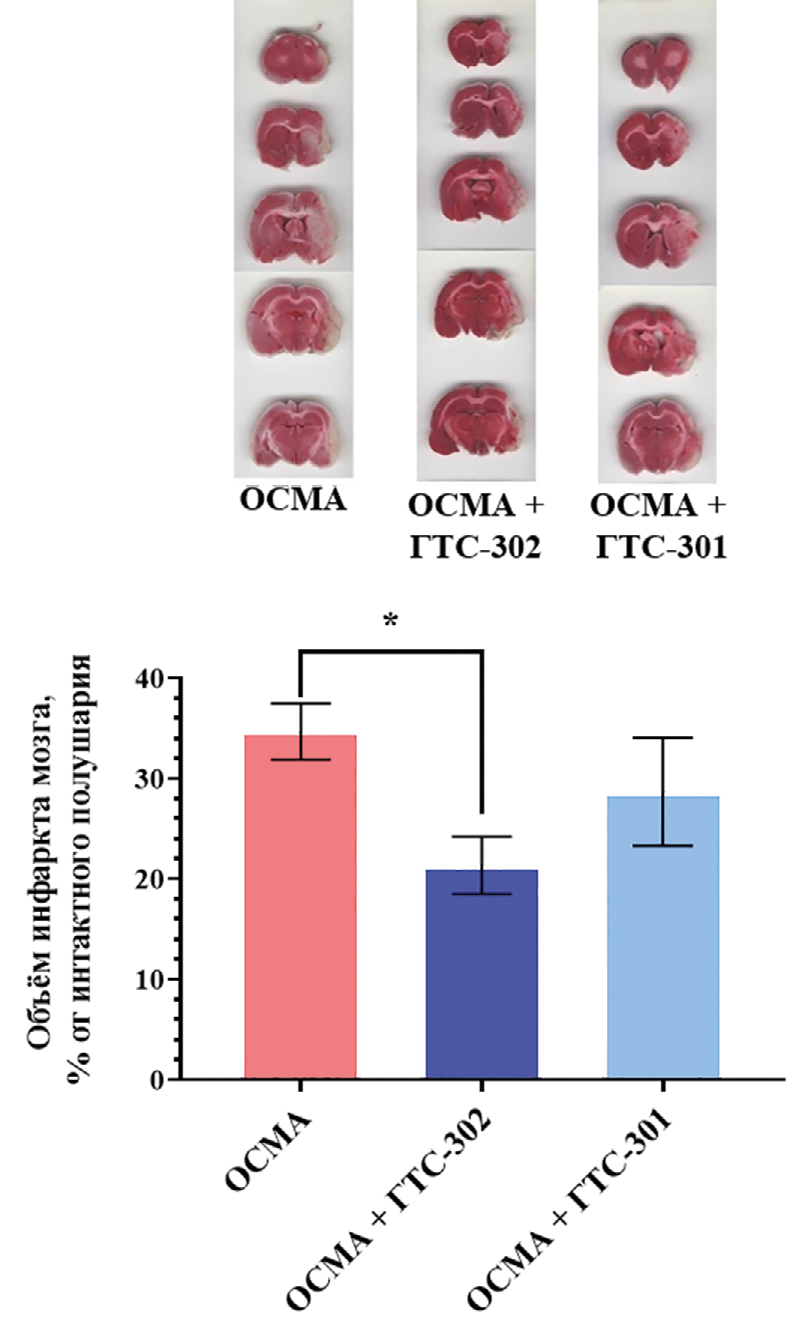
Рис. 3. Дипептид ГТС-302 (1 мг/кг, в/б, 7 дней) снижает объём инфаркта мозга на модели ишемического инсульта, индуцированного окклюзией средней мозговой артерии у крыс (ОСМА)
Примечания: Объём инфаркта мозга рассчитывали относительно объёма интактного полушария с поправкой на возможный отёк или атрофию ткани в ишемизированном полушарии по формуле, приведённой выше. Данные представлены в виде средних значений и стандартных ошибок средних. * — p = 0,048 по сравнению с группой «ОСМА» (критерий Краскела–Уоллиса с последующим тестом Данна).
Таким образом, было установлено, что дипептидный миметик 4-й петли NT-3 ГТС-302 обладает нейропротекторной активностью на модели ОСМА у крыс, снижая объём инфаркта мозга на 39 % на 7-е сутки после операции и улучшая неврологический статус крыс на 3-и сутки после операции. Согласно данным литературы [8], внутримозговое введение гена NT-3 в составе вирусного вектора до моделирования ОСМА способствует снижению инфаркта мозга на 36 % на 3-и сутки после операции и улучшению неврологического статуса с 1-х по как минимум 28-е сутки после операции. Сравнение эффектов ГТС-302 с полноразмерным нейротрофином показывает, что последний оказывает более выраженное корректирующее действие в отношении неврологических нарушений. Сходный по выраженности эффект ГТС-302 и NT-3 в отношении инфаркта мозга может быть связан с тем, что в случае NT-3 его оценивали в более ранние сроки после ОСМА.
Дипептид ГТС-301 оказался не активен в изученных условиях. Это может быть связано с тем, что в то время как ГТС-302 активирует все основные пострецепторные пути Trk-рецепторов — PI3K/Akt, MAPK/ERK и PLC-γ, ГТС-301 активирует только MAPK/ERK и PLC-γ [17]. Хорошо известно, что нейропротекторные эффекты нейротрофинов опосредованы главным образом PI3K/Akt сигнальным каскадом [7]. MAPK/ERK каскад также может быть вовлечён в нейропротекцию, но может и способствовать усилению нейродегенеративных процессов в патологических условиях, включая ишемию [23, 24]. Ранее нами было показано, что в ряду дипептидных миметиков NGF и BDNF нейропротекторную активность в условиях ОСМА у крыс проявляли только соединения, активирующие PI3K/Akt, при этом наиболее активные соединения, миметики 4-х петель NGF и BDNF, снижали объём инфаркта мозга примерно на 60 % [25]. Результаты настоящего исследования свидетельствуют в пользу необходимости активации PI3K/Akt и для проявления нейропротекторной активности миметиков NT-3 в условиях ОСМА.
Заключение
Дипептидный миметик 4-й петли NT-3 соединение ГТС-302, в спектре активации пострецепторного сигналинга которого присутствует PI3K/Akt каскад, проявляет нейропротекторную активность на модели ишемического инсульта, индуцированного ОСМА, у крыс. Дипептид ГТС-301, не активирующий PI3K/Akt каскад, не активен в тех же условиях.
Список литературы
1. Feigin VL, Brainin M, Norrving B, et al. World Stroke Organization: Global Stroke Fact Sheet 2025. Int J Stroke. 2025 Feb;20(2):132-144. doi: 10.1177/17474930241308142.
2. Houlton J, Abumaria N, Hinkley SFR, Clarkson AN. Therapeutic Potential of Neurotrophins for Repair After Brain Injury: A Helping Hand From Biomaterials. Front Neurosci. 2019 Aug 2;13:790. doi: 10.3389/fnins.2019.00790.
3. Sims SK, Wilken-Resman B, Smith CJ, et al. Brain-Derived Neurotrophic Factor and Nerve Growth Factor Therapeutics for Brain Injury: The Current Translational Challenges in Preclinical and Clinical Research. Neural Plast. 2022 Mar 2;2022:3889300. doi: 10.1155/2022/3889300.
4. Bothwell M. NGF, BDNF, NT3, and NT4. Handb Exp Pharmacol. 2014;220:3-15. doi: 10.1007/978-3-642-45106-5_1.
5. Wright DE, Snider WD. Neurotrophin receptor mRNA expression defines distinct populations of neurons in rat dorsal root ganglia. J Comp Neurol. 1995 Jan 16;351(3):329-38. doi: 10.1002/cne.903510302.
6. von Bartheld CS, Fritzsch B. Comparative analysis of neurotrophin receptors and ligands in vertebrate neurons: tools for evolutionary stability or changes in neural circuits? Brain Behav Evol. 2006;68(3):157-72. doi: 10.1159/000094085.
7. Skaper SD. The biology of neurotrophins, signalling pathways, and functional peptide mimetics of neurotrophins and their receptors. CNS Neurol Disord Drug Targets. 2008 Feb;7(1):46-62. doi: 10.2174/187152708783885174.
8. Zhang J, Shi Q, Yang P, et al. Neuroprotection of neurotrophin-3 against focal cerebral ischemia/reperfusion injury is regulated by hypoxiaresponsive element in rats. Neuroscience. 2012 Oct 11;222:1-9. doi: 10.1016/j.neuroscience.2012.07.023
9. Zhang WR, Kitagawa H, Hayashi T, et al. Topical application of neurotrophin-3 attenuates ischemic brain injury after transient middle cerebral artery occlusion in rats. Brain Res. 1999 Sep 18;842(1):211-4. doi: 10.1016/s0006-8993(99)01818-1.
10. Duricki DA, Hutson TH, Kathe C, et al. Delayed intramuscular human neurotrophin-3 improves recovery in adult and elderly rats after stroke. Brain. 2016 Jan;139(Pt 1):259-75. doi: 10.1093/brain/awv341.
11. Xiao QX, Chen JJ, Le Fang C, et al. Neurotrophins-3 plays a vital role in anti-apoptosis associated with NGF and BDNF regulation in neonatal rats with hypoxic-ischemic brain injury. Ibrain. 2020;6(2):12-17. doi:10.1002/j.2769-2795.2020.tb00047.x
12. Rocco ML, Soligo M, Manni L, Aloe L. Nerve Growth Factor: Early Studies and Recent Clinical Trials. Curr Neuropharmacol. 2018;16(10):14551465. doi: 10.2174/1570159X16666180412092859.
13. Kim S, Xu B, Merighi A. Brain-derived neurotrophic factor, nociception, and pain. Biomolecules. 2024 Apr 30;14(5):539. doi: 10.3390/biom14050539.
14. Gudasheva TA, Povarnina PY, Tarasiuk AV, Seredenin SB. Lowmolecular mimetics of nerve growth factor and brain-derived neurotrophic factor: Design and pharmacological properties. Med Res Rev. 2021 Sep;41(5):2746-2774. doi: 10.1002/med.21721.
15. Гудашева Т.А., Сазонова Н.М., Тарасюк А.В., и др. Первый дипептидный миметик нейротрофина-3: дизайн и фармакологические свойства. Доклады Академии наук. 2022;505(1):303-309. doi: 10.31857/S2686738922040059.
16. Tarasiuk AV, Sazonova NM, Melnikova MV, et al. Design and synthesis of a novel dipeptide mimetic of the 4th loop of neurotrophin-3 and its pharmacological effects. Mendeleev Commun. 2023;33(6):786-789. doi: 10.1016/j.mencom.2023.10.016.
17. Колик Л.Г., Константинопольский М.А., Николаев С.В., и др. Низкомолекулярные миметики нейротрофина-3, отличающиеся паттерном активации пострецепторного сигналинга, по-разному ослабляют проявления синдрома отмены морфина у крыс. Биохимия. 2024;89(11):1882-1892. doi: 10.31857/S0320972524110105. EDN: IKLOMW
18. Longa EZ, Weinstein PR, Carlson S, Cummins R. Reversible middle cerebral artery occlusion without craniectomy in rats. Stroke. 1989 Jan;20(1):84-91. doi: 10.1161/01.str.20.1.84.
19. Jolkkonen J, Puurunen K, Rantakömi S, et al. Behavioral effects of the alpha(2)-adrenoceptor antagonist, atipamezole, after focal cerebral ischemia in rats. Eur J Pharmacol. 2000 Jul 21;400(2-3):211-9. doi: 10.1016/s0014-2999(00)00409-x.
20. De Ryck M, Van Reempts J, Borgers M, et al. Photochemical stroke model: flunarizine prevents sensorimotor deficits after neocortical infarcts in rats. Stroke. 1989 Oct;20(10):1383-90. doi: 10.1161/01.str.20.10.1383.
21. Bederson JB, Pitts LH, Germano SM, Nishimura MC, Davis RL, Bartkowski HM. Evaluation of 2,3,5-triphenyltetrazolium chloride as a stain for detection and quantification of experimental cerebral infarction in rats. Stroke. 1986 Nov-Dec;17(6):1304-8. doi: 10.1161/01.str.17.6.1304.
22. Ingberg E, Dock H, Theodorsson E, et al. Effect of laser Doppler flowmetry and occlusion time on outcome variability and mortality in rat middle cerebral artery occlusion: inconclusive results. BMC Neurosci. 2018 Apr 19;19(1):24. doi: 10.1186/s12868-018-0425-0.
23. Gugliandolo A, Silvestro S, Sindona C, et al. MiRNA: Involvement of the MAPK Pathway in Ischemic Stroke. A Promising Therapeutic Target. Medicina (Kaunas). 2021 Oct 1;57(10):1053. doi: 10.3390/medicina57101053.
24. Schanbacher C, Bieber M, Reinders Y, et al. ERK1/2 Activity Is Critical for the Outcome of Ischemic Stroke. Int J Mol Sci. 2022 Jan 9;23(2):706. doi: 10.3390/ijms23020706.
25. Gudasheva T, Povarnina P, Dorofeev V. Dimeric dipeptide mimetics of neurotrophins as molecular tools and potential neuroprotective drugs. Explor Drug Sci. 2025;3:1008100. doi: 10.37349/eds.2025.1008100.
Об авторах
Д. М. НикифоровРоссия
Никифоров Дмитрий Михалович — м. н. с. лаборатории пептидных биорегуляторов отдела химии лекарственных средств.
Москва
П. Ю. Поварнина
Россия
Поварнина Полина Юрьевна — к. б. н., в. н. с. лаборатории пептидных биорегуляторов отдела химии лекарственных средств.
Москва
Т. А. Гудашева
Россия
Гудашева Татьяна Александровна — д. б. н., профессор, член-корреспондент РАН, руководитель отдела химии лекарственных средств.
Москва
Рецензия
Для цитирования:
Никифоров Д.М., Поварнина П.Ю., Гудашева Т.А. Изучение нейропротекторного действие дипептидных миметиков NT-3 соединений ГТС-301 и ГТС-302 на экспериментальной модели ишемического инсульта. Фармакокинетика и Фармакодинамика. 2026;(1):12-19. https://doi.org/10.37489/2587-7836-2026-1-12-19. EDN: LPQHXJ
For citation:
Nikiforov D.M., Povarnina P.Yu., Gudasheva T.A. Study of the neuroprotective effect of NT-3 dipeptide mimetics GTS-301 and GTS-302 on an experimental model of ischemic stroke. Pharmacokinetics and Pharmacodynamics. 2026;(1):12-19. (In Russ.) https://doi.org/10.37489/2587-7836-2026-1-12-19. EDN: LPQHXJ
JATS XML













































